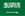1.Direkte dissociation og adsorption af vandmolekyler
På umættede metalsteder af metaloxider eller halvlederoxider (såsom Ti4+, Fe3+), adsorberer vandmolekyler først i molekylær form, efterfulgt af O-H-bindingsspaltning, hvilket resulterer i bro- eller terminale hydroxylgrupper (M-OH) og overfladehydrogenatomer. Den termodynamiske drivkraft i denne proces kommer fra den stærke Lewis surhed af metalioner, hvilket gør vandmolekyler nemme at adskille. Både eksperimenter og DFT-beregninger indikerer, at overflader dækket med lavt oxygenindhold har en tendens til at dissociere og adsorbere, mens overflader dækket med højt oxygenindhold har en tendens til at adsorbere molekyler.
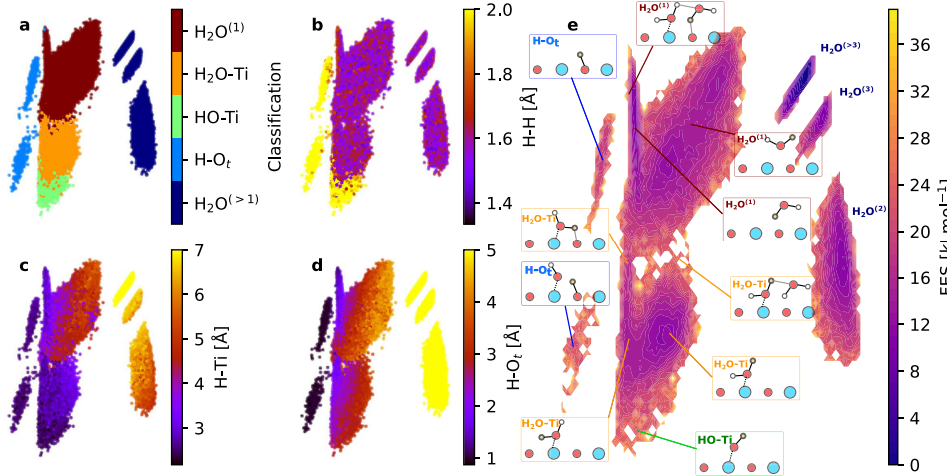
2.Oxygen ledighed (VO) medieret hydroxyl generation
Overflade ilt ledige steder giver elektroner, hvilket gør adsorberede vandmolekyler mere tilbøjelige til at dissociere. Efter at vandmolekyler adsorberer ved ledigheden, dannes to hydroxylgrupper, hvoraf den ene udfylder den tomme plads, og den anden hænger på det tilstødende metal. Denne mekanisme forklarer fænomenet med signifikant stigning i hydroxyldensitet under reducerende eller høje temperaturforhold og er tæt forbundet med ændringer i koordinationstallet for metalioner.
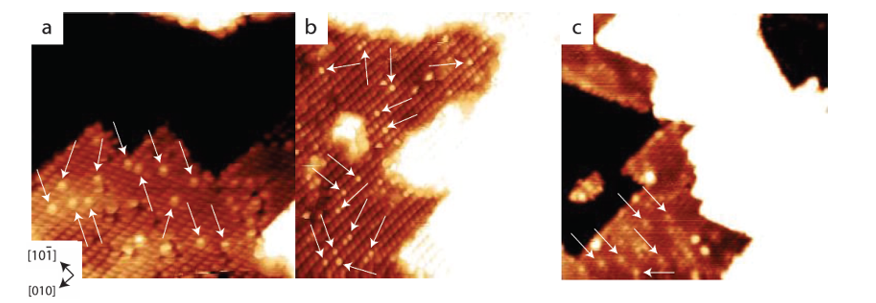
3. Hydrogen- eller brintatomoverløb
Ved metal/oxid-grænsefladen dissocierer H2 på metallet for at danne H ⁺/H ⁻, som derefter migrerer til overfladen af metaloxidet gennem hydrogenoverløb og danner hydroxylgrupper med overfladeoxygen. Denne proces blev direkte observeret i katalytiske systemer såsom lavtemperatur CO-oxidation, og hydrogenoverløb øgede signifikant hastigheden af overfladehydroxylgruppegenerering.
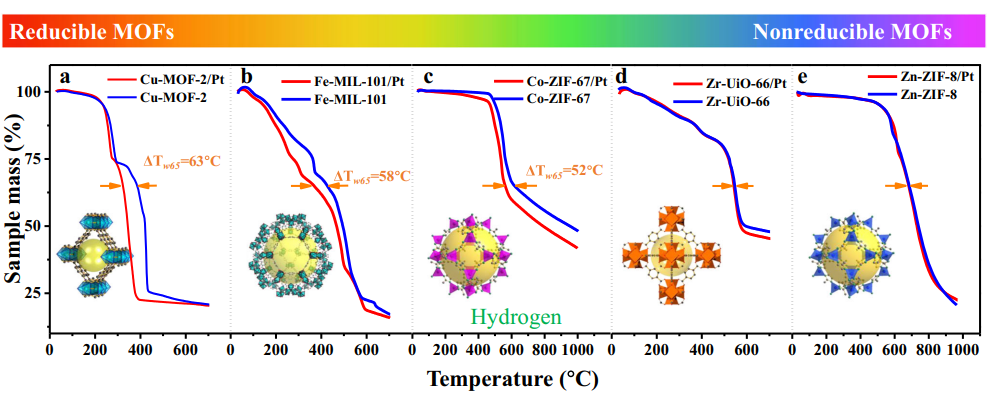
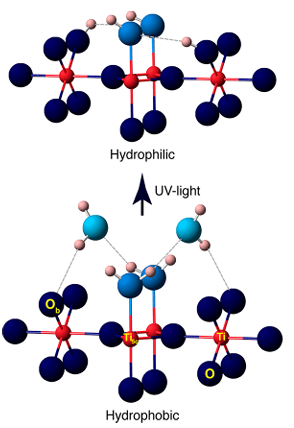
4. Fotokatalytisk/UV-induceret hydroxyldannelse
UV-lys exciterer halvledere såsom TiO2 for at generere elektronhulpar, som fanger overfladens oxygenatomer til dannelse af O ⁻ og derefter reagerer med adsorberede vandmolekyler eller hydroxylgrupper for at generere overflade OH ⁻, ledsaget af produktionen af hydroxylradikaler (· OH). Eksperimenter har vist, at UV-bestråling genererer yderligere ilttomheder på overfladen af TiO2, som yderligere reagerer med vand for at generere flere hydroxylgrupper, hvilket fører til fotoinduceret superhydrofilicitet.
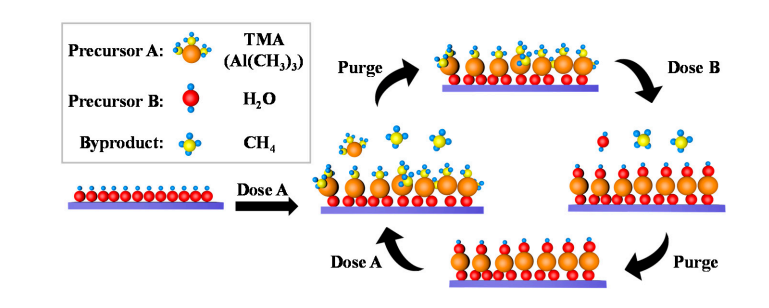
5. Dannelse af hydroxylgrupper på overfladen af aluminiumoxid
En lille mængde hydroxylgrupper findes naturligt på overfladen af aluminiumoxid, og vandmolekyler dissocierer og adsorberer på disse hydroxylgrupper og producerer nyt Al-OH. Under atomisk lagaflejring (ALD) gennemgår TMA (trimethylaluminium) koordinationsudveksling med overfladehydroxylgrupper for at danne Al-O-Al-bindinger og frigive methan; Efterfølgende reagerer vandpulsen igen med Al-O-bindinger for at regenerere overfladehydroxylgrupper, hvilket opnår cyklisk regenerering af hydroxylgrupper.
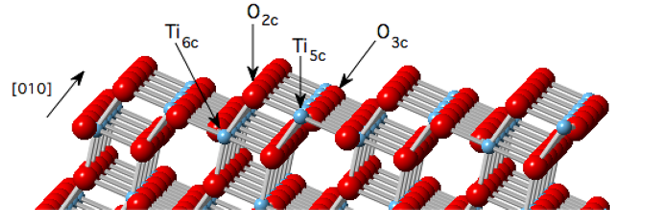
6.Overfladerekonstruktion - Metalmigrering fører til hydroxylaggregation
På krystaloverfladen af aluminiumoxid eller titaniumoxid migrerer lokale metalioner (såsom Al3+) til ledige overflader under høj temperatur eller højt hydrokemisk potentiale og danner hydroxylklynger af typen Al (OH) 3 eller Ti (OH) 3. Denne rekonstruktion er ledsaget af gitterforvrængning, hvilket gør adsorptionen af hydroxylgrupper på tilstødende vandmolekyler mere gunstig og danner et hydroxylbaselag med høj densitet.
7. Hydrolysemekanismen for hydroxylgrupper på siliciumoverfladen
Ved Si-O-Si-brobindingen kombinerer vandmolekyler med siliciumoxygenbindingen gennem synergistisk protonelektronoverførsel og danner Si-OH-grupper. Denne proces er særlig vigtig ved spændingskorrosion ved revnespidsen og overfladehydrolyse af glas, og forstærkningen af Si-OH-trækvibrationer blev direkte observeret ved eksperimentel infrarød spektroskopi.
SAT NANO er en bedste leverandør af nanopulver og mikropartikler i Kina, vi kan tilbyde kulstof nanorørpulver, som f.eks.
MWCNT-COOH,
MWCNT-OH, hvis du har nogen forespørgsel, er du velkommen til at kontakte os på sales03@satnano.com